美国CST中国公司(丁香通商铺)品牌商
13 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0
- 0
- 2
- 2
全部产品
- 查看全部分类
- Monoclonal Antibody(单克隆抗体)
- Polyclonal Antibody(多克隆抗体)
- Antibody Sampler kit(小包装套装)
- Antibody Duet(抗体对)
- 201709更新
- ChIP试剂盒
- Assay kit
- Biotinylated Peptide
- Blocking peptide
- Buffers
- Cell Extracts
- Cellular Dyes
- Chemical Modulators
- Detection system
- ELISA antibody pair
- ELISA kit
- Growth factors and cytokines
- HTScan Kinase Assay Kit
- IHC Control Slides
- IHC kit
- MW marker
- PhosphoPlus Antibody Kit
- Primer Set
- Protein Control
- Protein Kinase
- Protein Substrate
- PTMScan
- Secondary Antibody
- siRNA
- siRNA Kit
- 免疫组化抗体及配套试剂
- 蛋白翻译后修饰高通量筛选试剂盒和服务
- 磷酸化特异抗体
- 一抗
- 活动
致敬Hallmarks of Cancer 20周年,肿瘤研究产品买二赠一
询价
推荐产品

PathScan(R) RTK Signaling Antibody Array Kit (Chemiluminescent Readout)
品牌:Cell Signaling Technology
¥7893
咨询公司新闻/正文
CST专题介绍,助推细胞程序性死亡研究!(二)
2236 人阅读发布时间:2018-12-06 19:06
4. 细胞焦亡
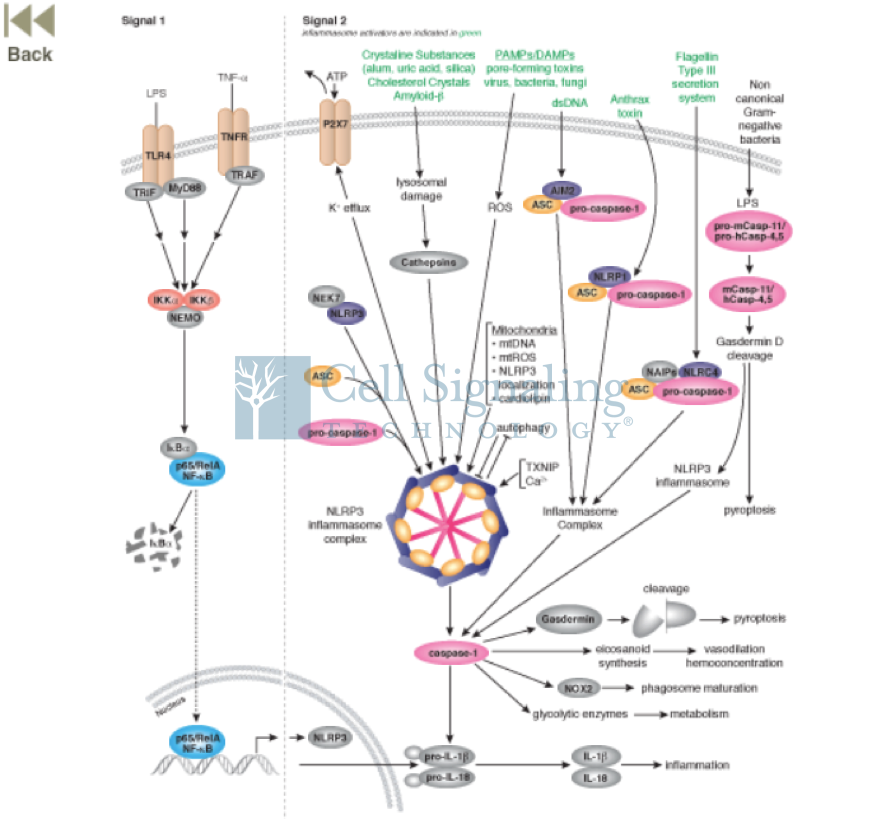
CST炎性小体(含细胞焦亡)研究相关产品:
若要了解更多焦亡相关蛋白,请点击互动式通路图,查询更多信号蛋白的研究背景和相关产品。
焦亡研究前沿及技术指导:
Webinar:细胞焦亡信号通路关键蛋白和研究动态
逐一突破:炎症 & 焦亡关键靶点 IL-1β,必须知道的5点!!!hot

图示:炎性小体的信号通路
细胞焦亡,一种炎性细胞程序性死亡过程,最初是在细胞感染过程中得以发现,后来被发现作为炎症小体(包含Caspase-1)及其他Caspase的下游,广泛参与多种疾病炎性过程中的细胞死亡过程。
当细胞受到外界微生物(如细菌)感染时,模式识别受体(pattern-recognition receptors, PRRs)可识别病原体相关分子模式(pathogen-associated molecular pattern,PAMP)或机体细胞释放的危险相关分子模式(danger-associated molecular pattern,DAMP),从而快速启动天然免疫反应以抵御病原微生物入侵。模式识别受体一般表达于巨噬细胞、单核细胞、树突状细胞、中性粒细胞、上皮细胞以及适应性免疫系统中的一些细胞。
模式识别受体依据亚细胞定位可分为两大类:(1)细胞膜上的Toll样受体(Toll-likereceptors,TLR)和C型凝集素受体(C-type lectin receptors);(2)细胞质内的RIG-Ⅰ样受体(RIG-Ⅰ-like receptors)、AIM2样受体(AIM2 like receptors)及NOD样受体(NOD-like receptors)。研究表明,位于细胞质内的一些NOD样受体/AIM2样受体在细胞内能够直接或者通过接头蛋白ASC(apoptosis-associated speck-like proteincontain a CARD)募集半胱氨酸天冬氨酸蛋白酶酶原(pro-Caspase-1),从而形成多蛋白复合体,即炎症小体(inflammasome),在机体天然免疫应答中起重要作用。识别不同病原体的PRRs组装为不同的炎症小体,目前研究报道最多的是NLRP3、NLRC4、NLRP1和AIM2炎症小体,NLRP2、NLRP6、NLRP7、NLRP12及IFI16等炎症小体也有报道。
经典的炎症小体活化过程是“双重信号”模型。初级信号为启动信号,细胞膜上的TLR识别胞外的危险相关分子模式或病原体相关分子模式,例如TLR4识别细菌脂多糖(LPS),激活NF-κB信号通路,诱导多种NOD样受体(例如NLRP3)蛋白以及pro-IL-1β/pro-IL-18的表达;次级信号为活化信号,细胞内的NOD样受体在迅速识别危险相关分子模式或病原体相关分子模式(例如线粒体DNA)后,与接头蛋白ASC组装,从而招募pro-Caspase-1。当pro-Caspase-1的局部浓度升高时,发生自体剪切,生成的片段p20和p10组成四聚体结构的具有生物活性的Caspase-1(即活化的Caspase-1)。炎症小体通过调控Caspase-1活化实现其功能:(1)Caspase-1剪切细胞因子pro-IL-1β和pro-IL-18使其成熟并释放到胞外介导炎症的级联反应,启动宿主免疫反应;(2)Caspase-1还可通过GasderminD(GSDMD)介导细胞焦亡(pyroptosis),表现为细胞膜崩解,胞质内毒素分子释放,从而趋化炎症细胞并促进其释放细胞因子,这一过程是经典的细胞焦亡激活过程。通过对细胞焦亡的研究的不断深入,一些新的分子机制被发现,比如一些新的Caspase(如Caspase-4、 Caspase-5、Caspase-11)可以被病原体结构分子(如LPS)直接激活,并通过GSDMD介导细胞焦亡,这一过程被称为非经典的细胞焦亡激活过程。
当细胞受到外界微生物(如细菌)感染时,模式识别受体(pattern-recognition receptors, PRRs)可识别病原体相关分子模式(pathogen-associated molecular pattern,PAMP)或机体细胞释放的危险相关分子模式(danger-associated molecular pattern,DAMP),从而快速启动天然免疫反应以抵御病原微生物入侵。模式识别受体一般表达于巨噬细胞、单核细胞、树突状细胞、中性粒细胞、上皮细胞以及适应性免疫系统中的一些细胞。
模式识别受体依据亚细胞定位可分为两大类:(1)细胞膜上的Toll样受体(Toll-likereceptors,TLR)和C型凝集素受体(C-type lectin receptors);(2)细胞质内的RIG-Ⅰ样受体(RIG-Ⅰ-like receptors)、AIM2样受体(AIM2 like receptors)及NOD样受体(NOD-like receptors)。研究表明,位于细胞质内的一些NOD样受体/AIM2样受体在细胞内能够直接或者通过接头蛋白ASC(apoptosis-associated speck-like proteincontain a CARD)募集半胱氨酸天冬氨酸蛋白酶酶原(pro-Caspase-1),从而形成多蛋白复合体,即炎症小体(inflammasome),在机体天然免疫应答中起重要作用。识别不同病原体的PRRs组装为不同的炎症小体,目前研究报道最多的是NLRP3、NLRC4、NLRP1和AIM2炎症小体,NLRP2、NLRP6、NLRP7、NLRP12及IFI16等炎症小体也有报道。
经典的炎症小体活化过程是“双重信号”模型。初级信号为启动信号,细胞膜上的TLR识别胞外的危险相关分子模式或病原体相关分子模式,例如TLR4识别细菌脂多糖(LPS),激活NF-κB信号通路,诱导多种NOD样受体(例如NLRP3)蛋白以及pro-IL-1β/pro-IL-18的表达;次级信号为活化信号,细胞内的NOD样受体在迅速识别危险相关分子模式或病原体相关分子模式(例如线粒体DNA)后,与接头蛋白ASC组装,从而招募pro-Caspase-1。当pro-Caspase-1的局部浓度升高时,发生自体剪切,生成的片段p20和p10组成四聚体结构的具有生物活性的Caspase-1(即活化的Caspase-1)。炎症小体通过调控Caspase-1活化实现其功能:(1)Caspase-1剪切细胞因子pro-IL-1β和pro-IL-18使其成熟并释放到胞外介导炎症的级联反应,启动宿主免疫反应;(2)Caspase-1还可通过GasderminD(GSDMD)介导细胞焦亡(pyroptosis),表现为细胞膜崩解,胞质内毒素分子释放,从而趋化炎症细胞并促进其释放细胞因子,这一过程是经典的细胞焦亡激活过程。通过对细胞焦亡的研究的不断深入,一些新的分子机制被发现,比如一些新的Caspase(如Caspase-4、 Caspase-5、Caspase-11)可以被病原体结构分子(如LPS)直接激活,并通过GSDMD介导细胞焦亡,这一过程被称为非经典的细胞焦亡激活过程。
CST炎性小体(含细胞焦亡)研究相关产品:
| 货号 | 产品名称 | 应用 | 反应性 |
| 3545 | Nod1 Antibody | W | H, M, R, Mk |
| 3793 | CIITA Antibody | W IP | H |
| 12421 | NLRC4 (D5Y8E) Rabbit mAb | W IP | H |
| 15101 | NLRP3 (D4D8T) Rabbit mAb | W IP | H, M |
| 13158 | NLRP3 (D2P5E) Rabbit mAb | W IP | H |
| 13829 | NLRX1 (D4M3Z) Rabbit mAb | W IP | H, M, R |
| 4990 | NALP1 Antibody | W | H, M, R |
| 12948 | AIM2 (D5X7K) Rabbit mAb | W IP | H |
| 13095 | AIM2 Antibody (Mouse Specific) | W IP | M |
| 13833 | TMS1 (E1E3I) Rabbit mAb | W IP | H |
| 67824 | ASC (D2W8U) Rabbit mAb (Mouse Specific) | W IP IF F | M |
| 2225 | Caspase-1 Antibody | W IHC | H |
| 3866 | Caspase-1 (D7F10) Rabbit mAb | W IP | H |
| 4199 | Cleaved Caspase-1 (Asp297) (D57A2) Rabbit mAb | W IP | H |
| 67314 | Cleaved Caspase-1 (Asp296) Antibody | W | M |
| 4450 | Caspase-4 Antibody | W | H |
| 46680 | Caspase-5 (D3G4W) Rabbit mAb | W IP | H |
| 14340 | Caspase-11 (17D9) Rat mAb | W IP | M |
| 12703 | IL-1β (D3U3E) Rabbit mAb | W IF F | H |
| 12242 | IL-1β (3A6) Mouse mAb | W IHC | H, M |
| 31202 | IL-1β (D6D6T) Rabbit mAb (Mouse Specific) | W F | M |
| 52718 | Cleaved-IL-1β (Asp117) Antibody (Mouse Specific) | W IP | M |
| 83186 | Cleaved-IL-1β (Asp116) (D3A3Z) Rabbit mAb | W IP IF | H |
| 96458 | Gasdermin D Antibody | W IP | H |
| 50928 | Cleaved Gasdermin D Antibody | W | H |
若要了解更多焦亡相关蛋白,请点击互动式通路图,查询更多信号蛋白的研究背景和相关产品。
焦亡研究前沿及技术指导:
Webinar:细胞焦亡信号通路关键蛋白和研究动态
逐一突破:炎症 & 焦亡关键靶点 IL-1β,必须知道的5点!!!hot





